| Bakanlık Adı | : | Sağlık Bakanlığından: |
| Tebliğ Adı | : | Kozmetik Ürün Bileşimlerinin Kontrolü İçin Gerekli Analiz Yöntemleri Hakkında Tebliğ (Tebliğ No:İEG-2005/7) |
| Tebliğ No | : | İEG-2005/7 |
| R. Gazete Tarihi | : | 01/07/200 |
| R. Gazete Sayısı | : | 2586 |
KOZMETİK ÜRÜN BİLEŞİMLERİNİN KONTROLÜ İÇİN GEREKLİ ANALİZ YÖNTEMLERİ
HAKKINDA TEBLİĞ
TEBLİĞ NO:İEG-2005/7
Amaç
Madde 1- Bu Tebliğin amacı, 2-fenoksietanol, 1-fenoksipropan-2-ol, metil, etil, propil, butil ve benzil, 4-hidroksibenzoat tanı ve tayini konularındaki analiz yöntemleri ile ilgili usul ve esasları belirlemektir.
Kapsam
Madde 2- Bu Tebliğ, aşağıdaki analiz metodlarının uygulamalarını kapsar:
2-fenoksietanol, 1-fenoksipropan-2-ol, metil, etil, propil, butil ve benzil
4-hidroksibenzoat tanı ve tayini Ek’teki yönteme göre yapılır.
Hukuki Dayanak
Madde 3 – Bu Tebliğ, 23/5/2005 tarihli ve 25823 sayılı Resmi Gazete’de yayımlanan Kozmetik Yönetmeliği’nin 16 ncı maddesine dayanılarak hazırlanmıştır.
Uyumlaştırılan Avrupa Birliği Mevzuatı
Madde 4 – Bu Tebliğ, 96/45/EEC sayılı Kozmetik Ürün Bileşimlerinin Kontrolü İçin Gerekli Analiz Yöntemleri Hakkında Yedinci Komisyon Direktifi dikkate alınarak Avrupa Birliği mevzuatına uyum kapsamında hazırlanmıştır. Bu Tebliğ, laboratuarların denenmiş ve bilimsel geçerliliği olan yöntemleri kullanmasını engellemez.
Yürürlük
Madde 5- Bu Tebliğ yayımı tarihinde yürürlüğe girer.
Yürütme
Madde 6- Bu Tebliğ hükümlerini Sağlık Bakanı yürütür.
EK
YÖNTEM – KOZMETİK ÜRÜNLERDE, 2-FENOKSİETANOL, 1-FENOKSİ- PROPAN-2-OL, METİL, ETİL, PROPİL, BUTİL VE BENZİL 4-HİDROKSİBENZOAT TANI VE TAYİNİ
A. TANI
1. KAPSAM VE UYGULAMA ALANI
Bu metod kozmetik ürünlerde, 2-fenoksietanol, 1-fenoksipropan-2-ol, metil 4- hidroksibenzoat, etil 4-hidroksibenzoat, propil 4-hidroksibenzoat, butil 4-hidroksibenzoat ve benzil 4-hidroksibenzoat’ın tanısına olanak sağlayan, “B” bölümünde belirtilen analiz metodu ile bağlantılı ince tabaka kromatografisi (TLC) prosedürünü tanımlar.
2. PRENSİP
Koruyucular, asitlendirilmiş kozmetik örnekten aseton ile ekstre edilir. Süzüldükten sonra, aseton solüsyonu su ile karıştırılır ve alkali ortamda yağ asitleri kalsiyum tuzları olarak çöktürülür. Alkali aseton / su karışımı, lipofilik maddeleri uzaklaştırmak için dietileter ile ekstre edilir.
Asitlendirildikten sonra koruyucular dietileter ile ekstre edilir. Dietileter ekstraktı silikajel kaplı ince tabaka plağına damlatılır. Plak yürütüldükten sonra kromatogram UV ışığı altında gözlenir ve Millon’s reaktifiyle görünür hale getirilir.
3. REAKTİFLER
3.1. Genel
Tüm çözeltiler analitik saflıkta olmalı ve kullanılan su, distile su veya eşdeğer kalitede olmalıdır.
3.2. Aseton
3.3. Dietileter
3.4. n-pentan
3.5. Metanol
3.6. Glasial asetik asit
3.7. Hidroklorik asit solüsyonu, c(HCl) = 4 mol / lt
3.8. Potasyum hidroksit solüsyonu c(KOH) = 4 mol / lt
3.9. Kalsiyum klorür dihidrat (CaCl2.2H2O)
3.10. Belirleme reaktifi: Millon’s reaktifi
Millon’s reaktifi (Merküri (II) nitrat) piyasada satışa hazır bir solüsyondur (Fluka 69820).
3.11. 2-fenoksietanol
3.12. 1-fenoksipropan-2-ol
3.13. Metil 4-hidroksibenzoat (metilparaben)
3.14. Etil 4-hidroksibenzoat (etilparaben)
3.15. n-propil 4-hidroksibenzoat (propilparaben)
3.16. n-butil 4-hidroksibenzoat (butilparaben)
3.17. Benzil 4-hidroksibenzoat (benzilparaben)
3.18. Referans solüsyonlar
3.11, 3.12, 3.13, 3.14, 3.15, 3.16 ve 3.17 referans maddelerinin her birinin % 0.1 (m/v) metanol içindeki solüsyonları hazırlanır.
3.19. Tank solvanı
88 hacim n-pentan (3.4) ile 12 hacim glasiyal asetik asit (3.6) karıştırılır.
4. EKİPMAN
Normal laboratuvar ekipmanı ve:
4.1. 60 oC’lik ısı elde etmeye yeterli su banyosu
4.2. Yürütme tankı (kağıt-filtresiz)
4.3. Ultraviyole ışık kaynağı, 254 nm
4.4. Konsantrasyon alanı ile 0.25 mm’lik 60 F254, silikajel ile kaplanmış, 20 cm x 20 cm.lik ince tabaka plakları (Merck No: 11798, Darmstadt veya eşdeğeri)
4.5. 105 oC’ye kadar ısı elde etmeye yeterli etüv
4.6. Kurutma makinası (sıcak)
4.7. Yün boya rulosu yaklaşık uzunluk : 10 cm, dış çap : 3.5 cm, yün tabakanın kalınlığı : 2 ile 3 mm olacaktır. Gerektiğinde yün inceltilebilir.
5.2 notuna bakınız.
4.8. Vidalı kapaklı 50 ml cam tüp
4.9. Elektrikli ısıtıcı tabla termostatlı, Isı ayarı: yaklaşık 80 oC. Sıcak tabla 20 x 20 cm ebadında ve sıcaklığın eşit şekilde dağılmasını sağlamak için yaklaşık 6 mm kalınlığında alüminyum plak ile kaplanmış olacaktır.
5. İŞLEM
5.1. Örnek hazırlanması
1 gr örnek 50 ml vidalı kapaklı cam tüp (4.8) içine tartılır. Üzerine dört damla hidroklorik asit solüsyonu (3.7) ve 40 ml aseton konulur.
Tuvalet sabunları gibi kuvvetli bazik kozmetik ürünler için 20 damla hidroklorik asit solüsyonu (3.7) ilave edilir. Tüp kapatılır. Aseton fazına koruyucuların ekstraksiyonlarını kolaylaştırmak için, karışım yaklaşık 60 oC’lik ısıda ve bir dakika boyunca kuvvetli bir şekilde çalkalanır.
PH kağıdı kullanılarak, solüsyonun pH’sı ölçülür, hidroklorik asit solüsyonu ile pH < 3’e ayarlanır, kuvvetlice bir dakika çalkalanır.
Solüsyon oda sıcaklığına kadar soğutulur. Filtre kağıdı ile erlene süzülür. Bu süzüntünün 20 ml’si 200 ml.lik bir erlene transfer edilir. Üzerine 60 ml su eklenir ve karıştırılır. PH indikatör kağıdı kullanılarak potasyum hidroksit (3.8) solüsyonu ile pH 10 civarına ayarlanır.
1 gr kalsiyum klorür dihidrat (3.9) eklenir ve kuvvetli bir şekilde çalkalanır. Solüsyon 75 ml dietileter içeren 250 ml’lik ayırma hunisi içine filtre kağıdından süzülür ve bir dakika boyunca kuvvetlice çalkalanır. Fazlar ayrılmaya bırakılır. 200 ml.lik erlene sulu faz toplanır. PH indikatör kağıdı kullanılarak hidroklorik asit solüsyonu ile pH yaklaşık 2’ye ayarlanır. Daha sonra 10 ml dietileter ilave edilir ve bir dakika boyunca kuvvetli bir şekilde çalkalanır. Fazlar ayrılmaya bırakılır. 5 ml.lik örnek şişesine yaklaşık 2 ml dietileter fazı transfer edilir.
5.2. İnce tabaka kromatografisi (TLC)
Isıtılmış alüminyum plaka (4.9) üzerine TLC plağı (4.4) yerleştirilir. Referans solüsyonları (3.18) her birinden 10 µl ve örnek solüsyondan (5.1) 100 µl TLC plağının konsantrasyon alanına damlatılır.
Eğer istenirse buharlaşmayı kolaylaştırmak için hava akımı kullanılır. Plak ısıtılmış plakadan alınır ve oda ısısına soğutulur. Tanka (4.2) 100 ml yürütme solvanı (3.19) aktarılır. Vakit geçirmeksizin plak önceden doyurulmamış tankta 15 cm yürütülür. Tanktan çıkarılır ve sıcak hava ile kurutulur.
Plak UV ışığı (4.3) altında incelenir ve lekelerin durumları işaretlenir. Fazla asetik asidi elimine etmek için, plak 30 dakika 100 oC ısıdaki etüv (4.5) içinde ısıtılır. Millon’s reaktifi (3.10) yardımıyla bu reaktif içine boyama rulosunu (4.7) daldırarak ve eşit şekilde nemlenmiş oluncaya kadar TLC plağının üstünde çevirerek kromatogram içindeki koruyucu lekelerinin görünür olması sağlanır.
NOT: Alternatif olarak, UV ışığı altında, açığa çıkan lekelerden her birinin üzerine dikkatli olarak bir damla millon’s reaktifi uygulanarak lekeler açığa çıkarılabilir.
4-hidroksibenzoik asit esterleri kırmızı lekeler, 2-fenoksietanol ve 1-fenoksipropan-2-ol esterleri sarı lekeler olarak görünürler. Bununla birlikte, 4-hidroksibenzoik asidin kendisi parabenlerin ayrıştırma ürünü veya koruyucu olarak örnekte bulunuyorsa, kırmızı leke olarak açığa çıkar (Bakınız 7.3 ve 7.4).
6. TANIMLAMA
Her leke için Rf değeri hesaplanır. Rf değeri gözönüne alınarak referans solüsyonları ile örnek solüsyonundan elde edilmiş lekeleri, UV ışığı altında ve lekelerin açığa çıkarılmalarından sonraki renkleri karşılaştırılır. Koruyucuların teşhisi hakkındaki ilk sonuçlar değerlendirilir.
Eğer parabenler mevcut ise, “B” bölümünde tanımlanan HPLC (Yüksek basınçlı sıvı kromatografi) prosedürü uygulanmak zorundadır. TLC kromatografisindeki ve yüksek basınçlı sıvı kromatografisindeki (HPLC) sonuçlar birleştirilerek 2-fenoksietanol, 1-fenoksipropan-2-ol ve parabenlerin varlığı kanıtlanır.
7. UYARILAR
7.1. Millon’s reaktifinin toksik olması nedeniyle, bu reaktif tanımlanmış prosedürlerden birine göre uygulanmak zorundadır. Spreyleme tavsiye edilmez.
7.2. Hidroksil grupları içeren diğer bileşikler aynı zamanda, millon’s reaktifi ile renklenebilirler.
Renklerin tablosu ve bu TLC prosedüründe kullanılan koruyucular için elde edilmiş Rf değerleri aşağıdaki yayınlarda bulunabilir.
N. de Kruijf, M.A.H. Rijk, L.A. Pranto-Soeteardhi ve A. Schouten (1987): Kozmetik ürünlerdeki koruyucuların tesbiti: Kozmetik ürünlerdeki koruyucuların tanısı ince tabaka kromatografi esesına dayanır (J. Chromatography 410, 395-411).
7.3. Aşağıdaki tablo elde edilebilir Rf değerlerinin listesini verir.
| Bileşikler | h Rf | Renk | |
| 4-hidroksibenzoik asit | 11 | Kırmızı | |
| Metilparaben | 12 | Kırmızı | |
| Etilparaben | 17 | Kırmızı | |
| Propilparaben | 21 | Kırmızı | |
| Butilparaben | 26 | Kırmızı | |
| Benzilparaben | 16 | Kırmızı | |
| 2-fenoksietanol | 29 | Sarı | |
| 1-fenoksipropan-2-ol | 50 | Sarı |
7.4. 4-hidroksibenzoik asit ve metilparaben için veya benzilparaben ve etilparaben için ayrılma elde edilmemiştir. Bu bileşiklerin tanımlanması, referans solüsyonları ve örnek solüsyonlarından elde edilmiş retansiyon zamanlarını karşılaştırarak bölüm B’de tanımlanan HPLC metodu uygulanarak doğrulanabilir.
B. TAYİN
1. KAPSAM VE UYGULAMA ALANI
Bu metod kozmetik ürünlerde 2-fenoksietanol, 1-fenoksipropan-2-ol, metil 4-hidroksibenzoat, etil 4-hidroksibenzoat, propil 4-hidroksibenzoat, butil 4-hidroksibenzoat ve benzil 4- hidroksibenzoat’ın tayinini tanımlar.
2. TANIM
Bu metoda göre tanımlanan koruyucuların miktarı yüzde kütle cinsinden ifade edilir.
3. PRENSİP
Sülfürik asit ile asitlendirilmiş örnek daha sonra etanol ve su karışımında bekletilir.
Ekstraksiyonu gerçekleştirmek için ortamdaki lipid fazın erimesi karışım hafifçe ısıtıldıktan sonra sağlanır ve süzülür.
Süzüntüdeki mevcut koruyucular internal standart olarak isopropyl 4-hidroksibenzoat kullanarak ters faz HPLC ile belirlenebilir.
4. REAKTİFLER
4.1. Genel
Bütün çözeltiler analitik saflıkta olmalı ve gerektiğinde HPLC için uygun olmalıdır. Kullanılan su damıtılmış olmalı yada eşdeğer saflıkta olmalıdır.
4.2. Absolu etanol
4.3. 2-Fenoksietanol
4.4. 1-Fenoksipropan-2-ol
4.5. Metil 4-hidroksibenzoat (metilparaben)
4.6. Etil 4-hidroksibenzoat (etilparaben)
4.7. n-propil 4-hidroksibenzoat (propilparaben)
4.8. Isopropil 4-hidroksibenzoat (isopropilparaben)
4.9. n-butil 4-hidroksibenzoat (butilparaben)
4.10. Benzil 4-hidroksibenzoat (benzilparaben)
4.11. Tetrahidrofuran
4.12. Metanol
4.13. Asetonitril
4.14. Sülfürik asit solüsyonu c(H2SO4) = 2 mol / lt
4.15. Etanol / su karışımı
Dokuz hacim etanol (4.2) ve bir hacim su
4.16. İnternal standart solüsyonu
Yaklaşık olarak tam tartılmış 0.25 g isopropilparaben (4.8), 500 ml.lik ölçülü balona alınır.
Etanol / su karışımı (4.15) ile çözülerek hacme tamamlanır.
4.17. Mobil faz: Tetrahidrofuran / su / metanol / asetonitril karışımı
5 hacim tetrahidrofuran, 60 hacim su, 10 hacim metanol ve 25 hacim asetonitril
4.18. Koruyucu stok solüsyonu
Yaklaşık olarak tam tartılmış 0.2 g 2-fenoksietanol, 0.2 g 1-fenoksipropan-2-ol, 0.05 g metilparaben, 0.05 g etilparaben, 0.05 g propilparaben, 0.05 g butilparaben ve 0.025 g benzilparaben 100 ml.lik ölçülü balona aktarılır. Etanol / su karışımı ile çözülür ve hacme tamamlanır.
Solüsyon, bir hafta buzdolabında stabil kalır.
4.19. Standart koruyucu solüsyon
Bir seri 50 ml.lik ölçülü balona stok solüsyondan (4.18) 20.00 ml, 10.00 ml, 5.00 ml, 2.00 ml ve 1.00 ml transfer edilir. Her balona 10 ml internal standart solüsyonu (4.16) ve 1 ml sülfürik asit solüsyonu (4.14) eklenir ve etanol / su karışımı ile hacme tamamlanır. Bu solüsyonlar taze hazırlanmalıdır.
5. EKİPMAN
Normal laboratuvar ekipmanı ve:
5.1. 60oC ± 1oC’lik ısı elde etmeye yeterli su banyosu
5.2. Yüksek basınçlı sıvı kromatografi cihazı: UV-dedektörlü, dalga boyu 280 nm.
5.3. Analitik Kolon:
Paslanmaz çelik, 25 cm x 4.6 mm (veya 12.5 cm x 4.6 mm) Nucleosil 5C18 veya eşdeğeri
(Bakınız 10.1)
5.4. Vidalı kapaklı 100 ml.lik cam tüpler
5.5. Kaynamayı kolaylaştırmak için carborundum parçaları, boyutları 2 ile 4 mm veya eşdeğeri
6. İŞLEM
6.1. Örnek hazırlama
6.1.1. İnternal standart ilave edilmeden örnek hazırlama
Yaklaşık olarak tam tartılmış 1 g örnek vidalı kapaklı tüpe aktarılır. 1 ml sülfürik asit solüsyonu (4.14) ve 50 ml etanol / su karışımı (4.15) ilave edilir. Yaklaşık 1 gr kaynatma parçası (5.5) eklenir, tüpün kapağı kapatılır, homojen bir süspansiyon elde edilinceye kadar kuvvetli bir şekilde çalkalanır (En az bir dakika). Tüp koruyucuların etanol fazına ekstraksiyonunu kolaylaştırmak için 5 dakika süresince 60oC ± 1oC’lik su banyosunda (5.1) tutulur.
Tüp hemen soğuk su altında soğutulur ve bir saat boyunca buzdolabında muhafaza edilir.
Filtre kağıdından süzülür. Yaklaşık 2 ml süzüntü 5 ml.lik örnek şişesine transfer edilir.
Süzüntüler buzdolabında muhafaza edilir ve 24 saat içinde HPLC’de tayin edilir.
6.1.2. İnternal standart ilave ederek örnek hazırlama
Yaklaşık 1 g ± 0.1 g örnek 100 ml.lik vidalı kapaklı cam tüpe tartılır.
1 ml sülfürik asit solüsyonu ve 40 ml etanol / su karışımı tüpe pipetlenir. Yaklaşık 1 g kaynatma parçası (5.5) ve tam olarak 10 ml internal standart solüsyonu eklenir. Tüp kapatılır, homojen bir süspansiyon elde edilinceye kadar şiddetle çalkalanır (En az 1 dakika). Tüp, koruyucuların etanol fazına ekstraksiyonlarını kolaylaştırmak için 5 dakika süresince 60oC ±1oC’lik su banyosunda bırakılır.
Tüp hemen soğuk su altında soğutulur ve 1 saat boyunca buzdolabında muhafaza edilir. Süzgeç kağıdından süzülür.
Yaklaşık 2 ml süzüntü 5 ml.lik örnek şişesine transfer edilir (Test solüsyonu). Süzüntü buzdolabında muhafaza edilir ve 24 saat içinde HPLC’de tayin edilir.
6.2. Yüksek basınçlı sıvı kromatografisi (HPLC)
6.2.1. Kromatografik şartlar
− Mobil faz : Tetrahidrofuran / su / metanol / asetonitril karışımı (4.17)
− Akış hızı : 1.5 ml / dakika
− Dalga boyu : 280 nm
6.2.2. Kalibrasyon
Standart koruyucu solüsyonların (4.19) her birinden 10 µl enjekte edilir. Buradan elde edilen kromatogramlardan, koruyucu standart solüsyonlarının pik yüksekliğinin internal standart pik yüksekliğine oranı hesaplanır. Bu orana karşı koruyucu konsantrasyonlar grafiğe geçirilir.
6.2.3. Tayin
Kromatografa, internal standartsız 10 µl örnek solüsyon (6.1.1) enjekte edilir, kromatogram kaydedilir.
Koruyucu standart solüsyonların (4.19) birinden 10 µl enjekte edilir ve kromatogram kaydedilir. Elde edilen kromatogramlar karşılaştırılır.
Örnek ekstraktın (6.1.1) kromatogramında hiçbir pikin isopropilparaben’-inkine (önerilen internal standardı) yaklaşık aynı alıkonma zamanı göstermemesi durumunda, internal standart (6.1.2) içeren 10 µl örnek solüsyon enjekte edilir. Kromatogram kaydedilir ve pik yükseklikleri ölçülür.Örnek solüsyonun kromatogramında isopropilparabene yaklaşık aynı alıkonma zamanına sahip pik gözlenmesi durumunda, diğer bir internal standart seçilmek zorundadır.
İnceleme sırasında, koruyuculardan birinin örnek solüsyonda olmaması durumunda, bu koruyucu alternatif internal standart olarak kullanılabilir.
Araştırılan koruyucuların pik yüksekliklerinin internal standart pik yüksekliğine oranları hesaplanır.
Kalibrasyon prosedüründe kullanılan standart solüsyonlar için lineer bir cevap elde edilmiş olmasından emin olunmalıdır.
Standart solüsyonlar ve örnek solüsyonlar için elde edilmiş kromatogramların aşağıdaki gerekliliklere uymasından emin olunmalıdır.
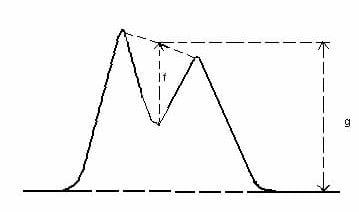
− En kötü ayrılmış pik çiftlerinin seperasyonu en azından 0.90 olmak zorundadır (Pik seperasyonu tanımı için şekil 1’e bakınız).
| Pik seperasyonu (p) | ||
| p = f/g | ||
 | ||
| Şekil 1: Pik seperasyonu |
İstenilen seperasyona ulaşılmaması durumunda, ya daha etkili kolon kullanılması veya özelliklere uygun oluncaya kadar mobil faz oranlarının ayarlanması gerekli olacaktır.
− Elde edilen tüm pikler için asimetri faktörü As 0.9 ile 1.5 arasında olacaktır (Pik asimetri faktörü tanımı için Şekil 2’ye bakınız). Asimetri faktörü tayini için kromatogram kaydedilirken, kağıt hızı en az 2 cm / dakika olarak önerilmiştir.
| Asimetri faktörü (As) | |
| As = b/a | |
 | |
| Şekil 2: Pik asimetri faktörü |
− Sabit temel çizgi elde edilecektir.
7. HESAPLAMA
Kalibrasyon eğrisi (6.2.2) örnek solüsyondaki koruyucuların konsantrasyonunun hesaplanması için kullanılır. 2-fenoksietanol, 1-fenoksipropan-2-ol, metil 4-hidroksibenzoat, etil 4-hidroksibenzoat, propil 4-hidroksibenzoat, butil 4-hidroksibenzoat ve benzil 4- hidroksibenzoat içerikleri, wi aşağıdaki formül kullanılarak % ağırlık (% m/m) olarak hesaplanır:
| bi | |
| % wi (m/m)= | |
| 200 x a |
Burada:
bi : Kalibrasyon eğrisinden okunan test solüsyonundaki i koruyucu sunun konsantrasyonu (µg / ml)
a : Test miktarının kütlesi (g)
8. TEKRARLANABİLİRLİK (ISO NORM 5725)
Alıkonma süresi: r10.5’deki uyarılarak bakınız.
9. ÜRETİLEBİLİRLİK (ISO NORM 5725)
(Pik yüksekliği: R)
10.5’deki uyarılara bakınız.
10. UYARILAR
10.1 Sabit faz
Maddelerin alıkonma süreleri HPLC kolonunun tipine, markasına, dolgu maddesine bağlıdır.
Önerilen kolonlara alternatif olarak Hypersil ODS veya Zorbax ODS kullanılabilir. Ayrıca önerilen mobil faz kompozisyonu uygun ayırım elde edebilmek için değiştirilebilir.
10.2 Dalga boyu
Dalga boyunda küçük değişmeler bile tayinde belirgin değişikliğe neden olabilir.
Bunun için analiz süresince bu parametre kontrol edilmelidir.
10.3 Etkileşimler
Tanımlanan şartlarda başka maddeler de (kozmetik katkı maddeleri, koruyucular gibi) kolonda sürüklenecektir.
10.4 Kolonu korumak için uygun bir ön-kolon kullanılabilir.
10.5 Bu metod 9 laboratuvar arasında kollaboratif çalışmaya sunulmuş olup, aşağıdaki tablo her 3 örnek için % kütle cinsinden bileşenlerin “r” ve “R” değerlerini vermektedir.
| Örnek | 2-fenoksi etanol | 1-fenoksi propan-2-ol | Metil paraben | Etil paraben | Propil paraben | Butil paraben | Benzil paraben | |
| Vitaminli Krem | m r R | 1.124 0.016 0.176 | 0.250 0.018 0.030 | 0.0628 0.0035 0.0068 | 0.031 0.0028 0.0111 | 0.0906 0.0044 0.0034 | ||
| Az yağlı Krem | m r R | 1.196 0.040 0.147 | 0.266 0.003 0.022 | 0.076 0.002 0.004 | ||||
| Masaj Kremi | m r R | 0.806 0.067 0.112 | 0.180 0.034 0.078 | 0.148 0.013 0.012 | 0.152 0.015 0.016 | |||
Kaynak: IEGM